多発性単ニューロパチーの症状を主訴に脳神経内科を初診し、アレルギー素因+著明な好酸球上昇+他臓器障害から診断に至ることが多いです。診断は比較的容易ですが、血管炎による末梢神経障害は虚血性の病態機序で生じるため緊急性が非常に高く、早急な評価(可能であれば生検も含めて)・治療開始が重要です。肺・心・腎など重要臓器の障害も併存しうることから、全身臓器の評価・フォローも忘れてはいけません。
病態
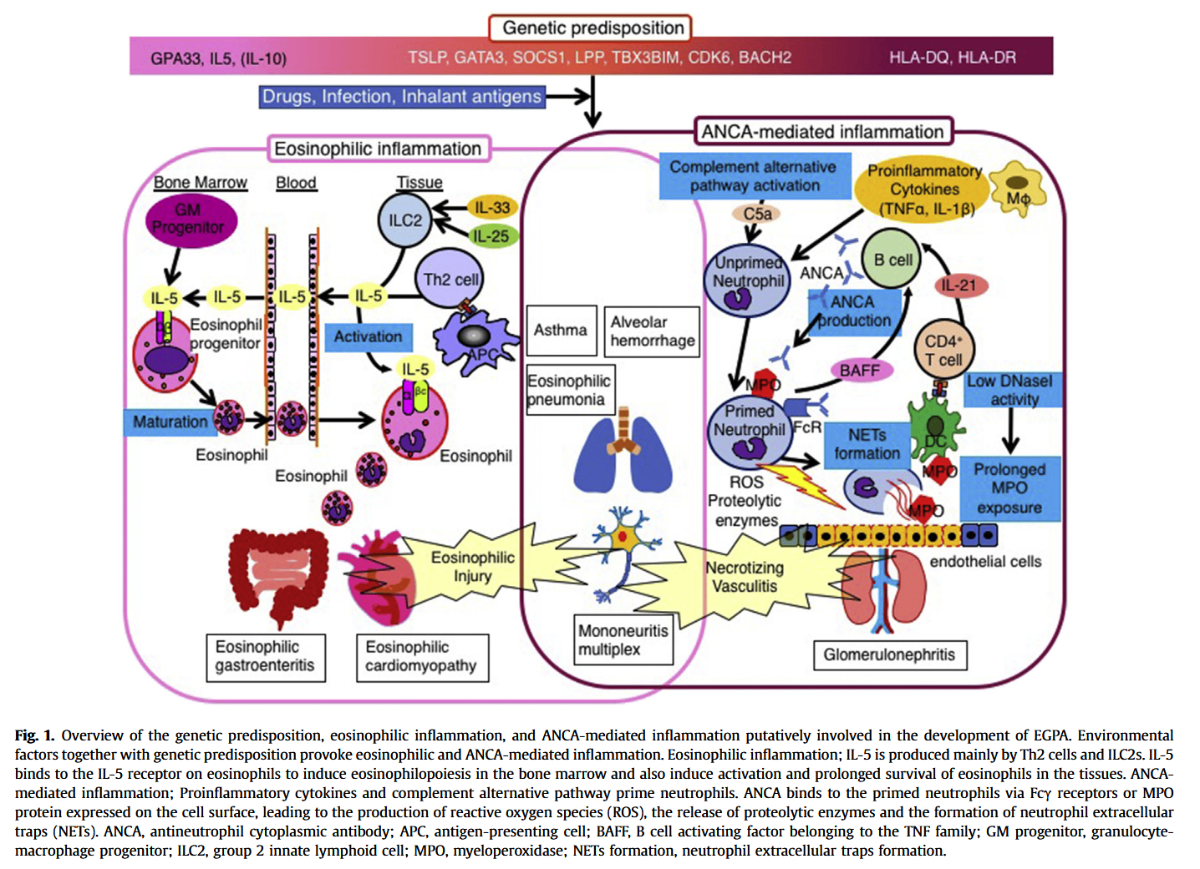
*Allergol Int. 2019;68(4):430-436.
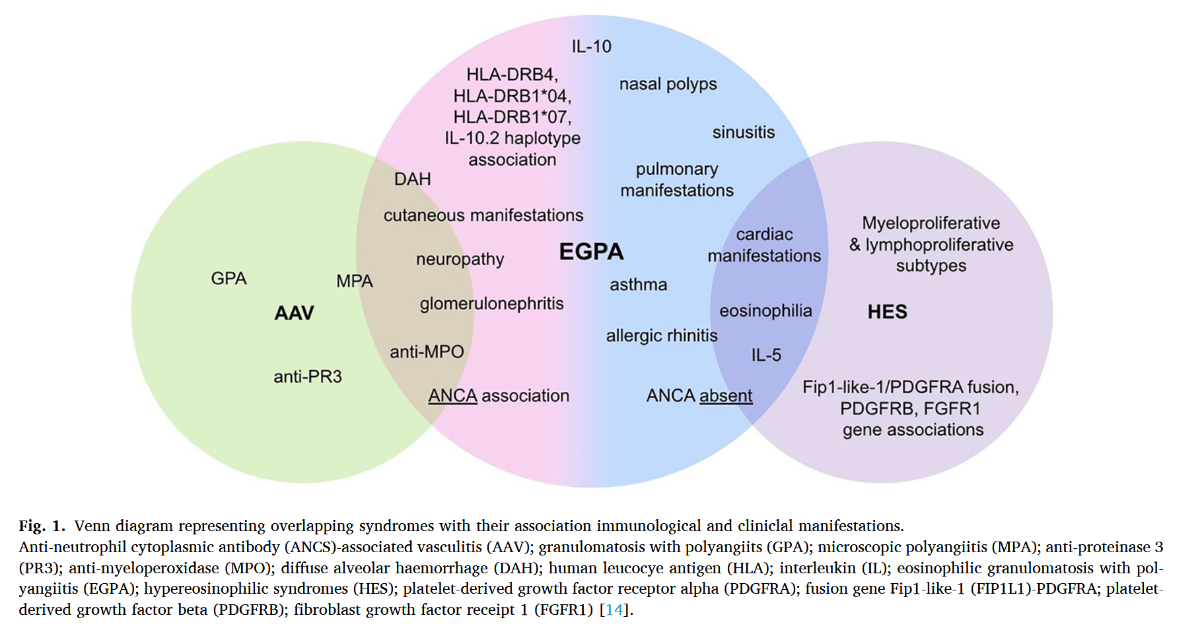
*Autoimmun Rev. 2023;22(1):103219.
免疫異常
- 好酸球性炎症
-
何らかのアレルゲンによりアレルギー反応が惹起され、好酸球が過剰に増殖する。
組織へ浸潤し、炎症性サイトカインなどの放出により炎症を引き起こし、組織障害をきたす。
気管支喘息・好酸球性肺炎・好酸球性心筋症・好酸球性胃腸炎など。
- 抗好中球細胞質抗体(ANCA:anti-neutrophil cytoplasmic antibody)
-
好中球を活性化することで血管炎を引き起こし、血流障害を介して虚血性の臓器障害をきたす。
皮膚潰瘍・多発単神経炎・糸球体腎炎・肺胞出血・脳血管障害・虚血性腸炎など。
遺伝的要因
家族内発生が国内外から報告されている。
EGPA患者でHLA-DRB1*07とHLA-DRB4が多いとの報告あり。
疫学
100万人あたり12-15例程度の有病率。
ANCA関連血管炎の中で約10%を占める。
診断時の平均年齢:40-50歳。有意な性差なし。
臨床症候
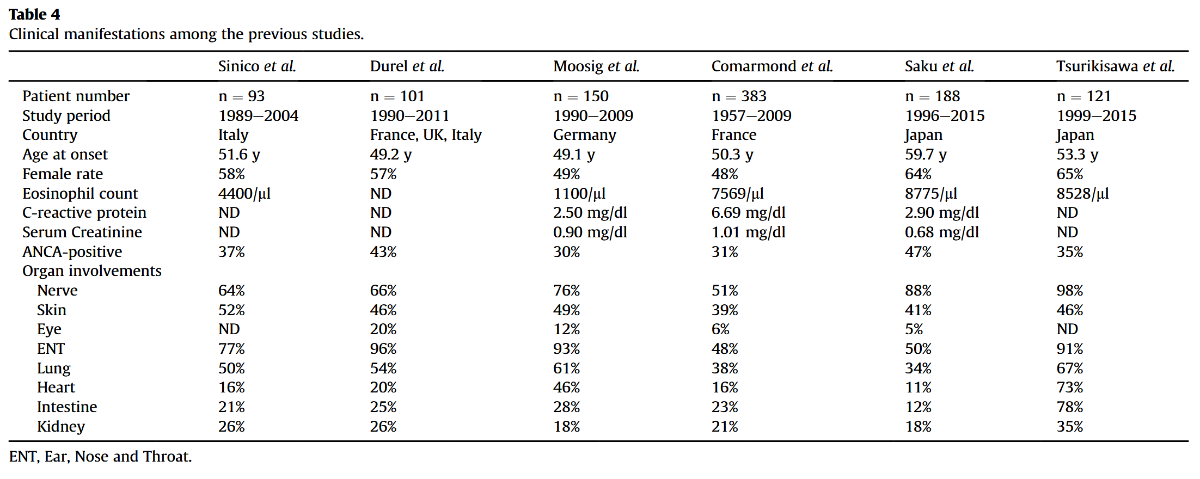
*Allergol Int. 2019;68(4):430-436.
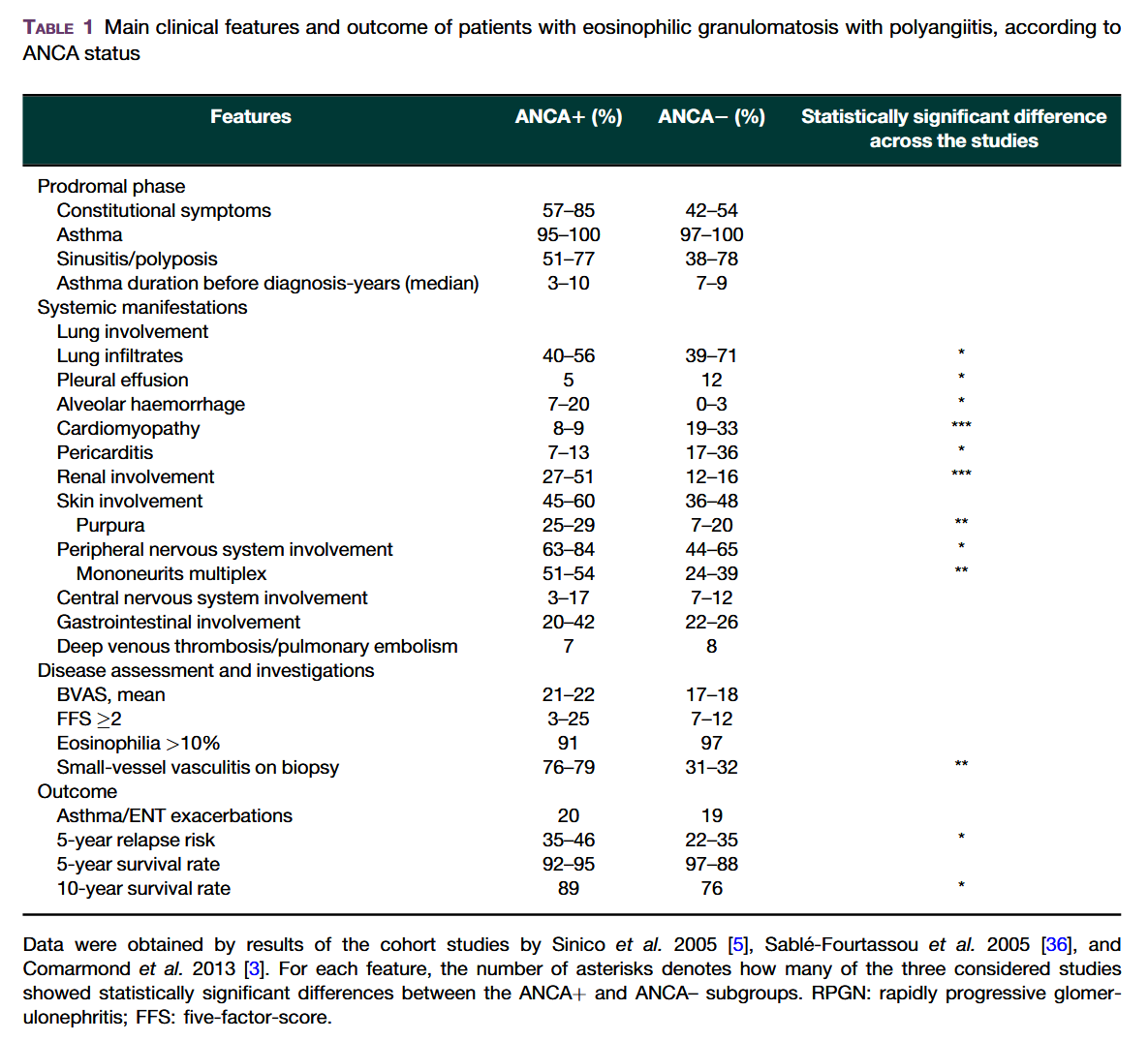
*Rheumatology. 2020;59(Suppl 3):iii84-iii94.
ANCA陽性例と陰性例で臨床症候の特徴が異なる。
経過
- Prodromal phase:前駆期
-
気管支喘息・アレルギー性鼻炎・好酸球性副鼻腔炎を含むアトピー性疾患の発症。
末梢血好酸球増加症と同時に発生することもある。
- Eosinophilic phase:好酸球増多期
-
末梢血好酸球増加症、肺・消化管など各種臓器への好酸球浸潤がみられる。
- Vasculitic phase:血管炎期
-
非特異的症状(発熱・体重減少・倦怠感など)によって発症する。
中小血管の炎症により、多臓器障害が起こる。
全身症状
発熱・関節痛・筋肉痛・体重減少など。
臓器障害
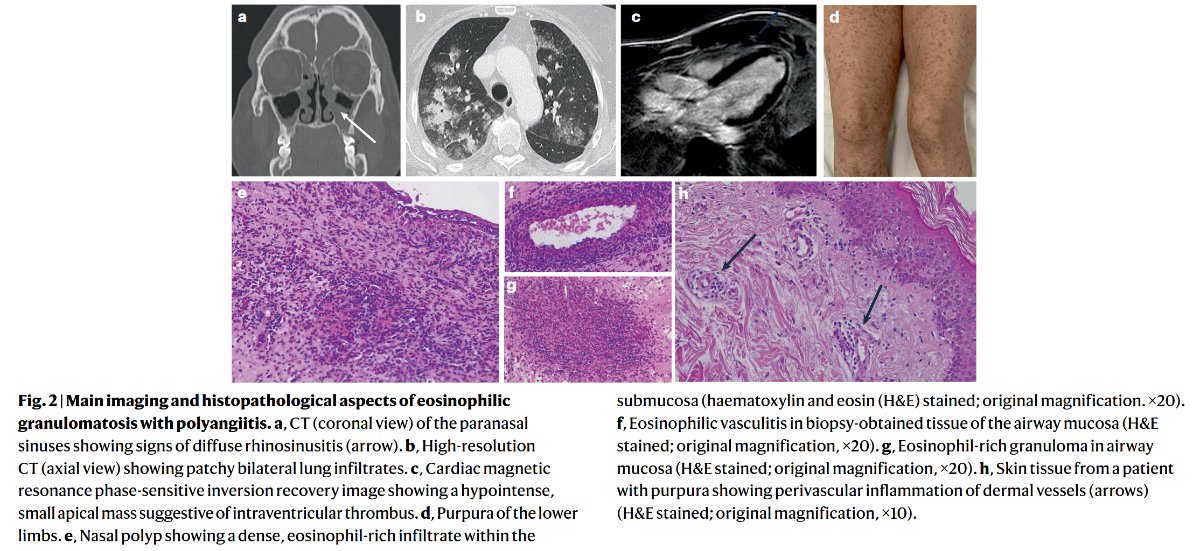
*Nat Rev Rheumatol. 2023;19(6):378-393.
- 末梢神経障害
-
典型的には多発性単神経炎。疼痛・しびれ・脱力。
対称性多発神経炎(24%)・非対称性多発神経炎(3%)・神経根症(3%)の報告もあり。
- 中枢神経系障害
-
まれ。脳卒中(脳梗塞・くも膜下出血・脳出血)。
- 皮膚
-
血管炎期に頻度が高い症状の1つ。
点状出血・紫斑・斑状出血・水疱性病変・蕁麻疹・紅斑。
有痛性皮下結節:病理所見は肉芽腫
耳・鼻・咽頭・喉頭-
アレルギー性鼻炎・再発性副鼻腔炎・鼻ポリープ。
慢性中耳炎・感音性難聴がみられることもある。
上咽頭・上気道の壊死性病変は、多発血管炎性肉芽腫症(GPA)に特徴的ではあるが、EGPAではまれ。
- 気管支
-
気管支喘息は明らかな血管炎に約8-10年先行する。
吸入ステロイド・長時間作用型β作動薬の使用によっても病状コントロールが不良であることが多い。
- 肺
-
好酸球性肺炎様の病変(移動性・散在性・末梢優位のすりガラス影)。
結節・肉芽腫病変や肺胞出血は比較的まれ。
- 心血管
-
心筋症・心膜炎・心不全
- 腎臓
-
急速進行性糸球体腎炎
- 消化管
-
好酸球性胃腸炎・虚血性腸炎
腹痛・下痢・消化管出血をきたす。
検査
血液検査
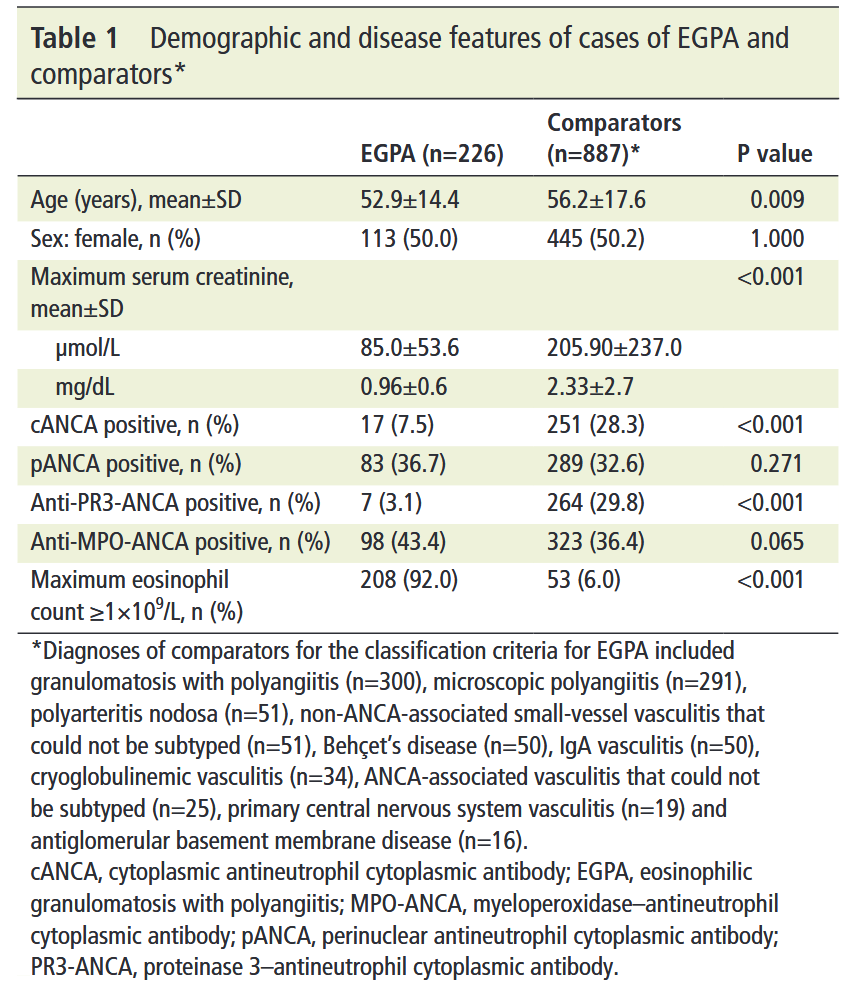
*Ann Rheum Dis. 2022;81(3):309-314.
好酸球:1,000/μL以上(または総白血球数の10%以上)
IgE:EGPA患者の75%で上昇あり。
抗好中球細胞質抗体(ANCA):MPO-ANCA(p-ANCA)がEGPA患者の30-40%で陽性となる。
急性期反応:CRP・赤沈
その他:正球性正色素性貧血・高ガンマグロブリン血症・IgG4上昇・リウマチ因子陽性・抗核抗体陽性・補体上昇
鑑別:寄生虫検査・HIV・ビタミンB12・末梢血塗抹標本(芽球・異型好酸球)
心評価
スクリーニング:血液検査(心筋トロポニン・NT-proBNP)・心電図・経胸壁心エコー(壁運動異常・壁在血栓・弁膜症)
異常があれば、造影MRI・心筋生検
その他の臓器障害
血清Cr・BUN・尿検査
CT:肺・副鼻腔の病変評価
肺機能検査・気管支鏡検査
神経伝導検査:末梢神経障害
脳MRI:中枢神経系障害
腹部症状:上下部消化管内視鏡検査
病理検査
可能なら組織学的確認が望ましい。
有意な検体が得られる可能性が高く、最も侵襲性が低い選択肢を選ぶ。
皮膚・神経症状があれば、いずれかの検体採取が望ましい。
鼻・副鼻腔粘膜生検:感度35%と報告あり。
肺:経気管支肺生検よりも胸腔鏡下または開胸肺生検が望ましい。
診断
厚生労働省によるEGPAの分類基準(1998年)
- 主要臨床所見
- 気管支喘息あるいはアレルギー性鼻炎
- 好酸球増加
- 血管炎による症状:発熱(38℃以上・2週間以上)、体重減少(6か月以内に6kg以上)、多発性単神経炎、消化管出血、多関節痛(炎)、筋肉痛(筋力低下)、紫斑のいずれか1つ以上
- 臨床経過の特徴:主要臨床所見Ⅰ・Ⅱが先行し、Ⅲが発症する。
- 主要組織所見
- 周囲組織に著明な好酸球浸潤を伴う細小血管の肉芽腫性またはフィブリノイド壊死性血管炎の存在
- 血管外肉芽腫の存在
- 診断のカテゴリー
- Definite
- 1.主要臨床所見3項目を満たし、3.主要組織所見の1項目を満たす場合。
- 1.主要臨床所見3項目を満たし、2.臨床経過の特徴を示した場合。
- Probable
- 1.主要臨床所見1項目を満たし、3.主要組織所見の1項目を満たす場合。
- 1.主要臨床所見3項目を満たすが、2.臨床経過の特徴を示さない場合。
- Definite
- 参考となる所見
- 白血球増加(≧1万/μL)
- 血小板増加(≧40万/μL)
- 血清IgE増加(≧600U/mL)
- MPO-ANCA陽性
- リウマトイド因子陽性
- 肺浸潤陰影
2022年ACR/EULAR分類基準
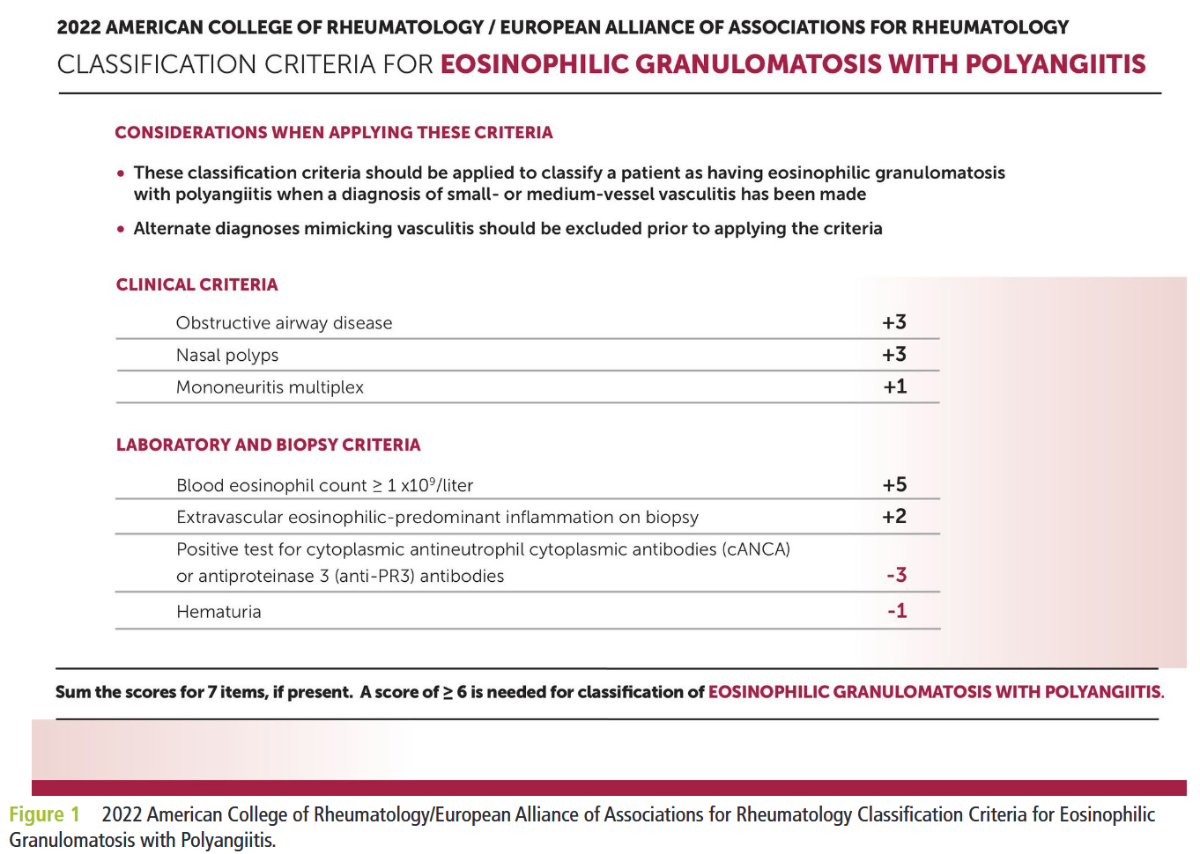
*Ann Rheum Dis. 2022;81(3):309-314.
鑑別疾患
NSAIDs過敏喘息・アスピリン喘息(AERD)
慢性好酸球性肺炎
アレルギー性気管支肺アスペルギルス症
好酸球増加症候群(HES)
その他の血管炎:多発血管炎性肉芽腫症・顕微鏡的多発血管炎
その他の好酸球性疾患:薬剤性・トキソカラ症・HIV感染症・腫瘍随伴症
治療
国内ガイドライン
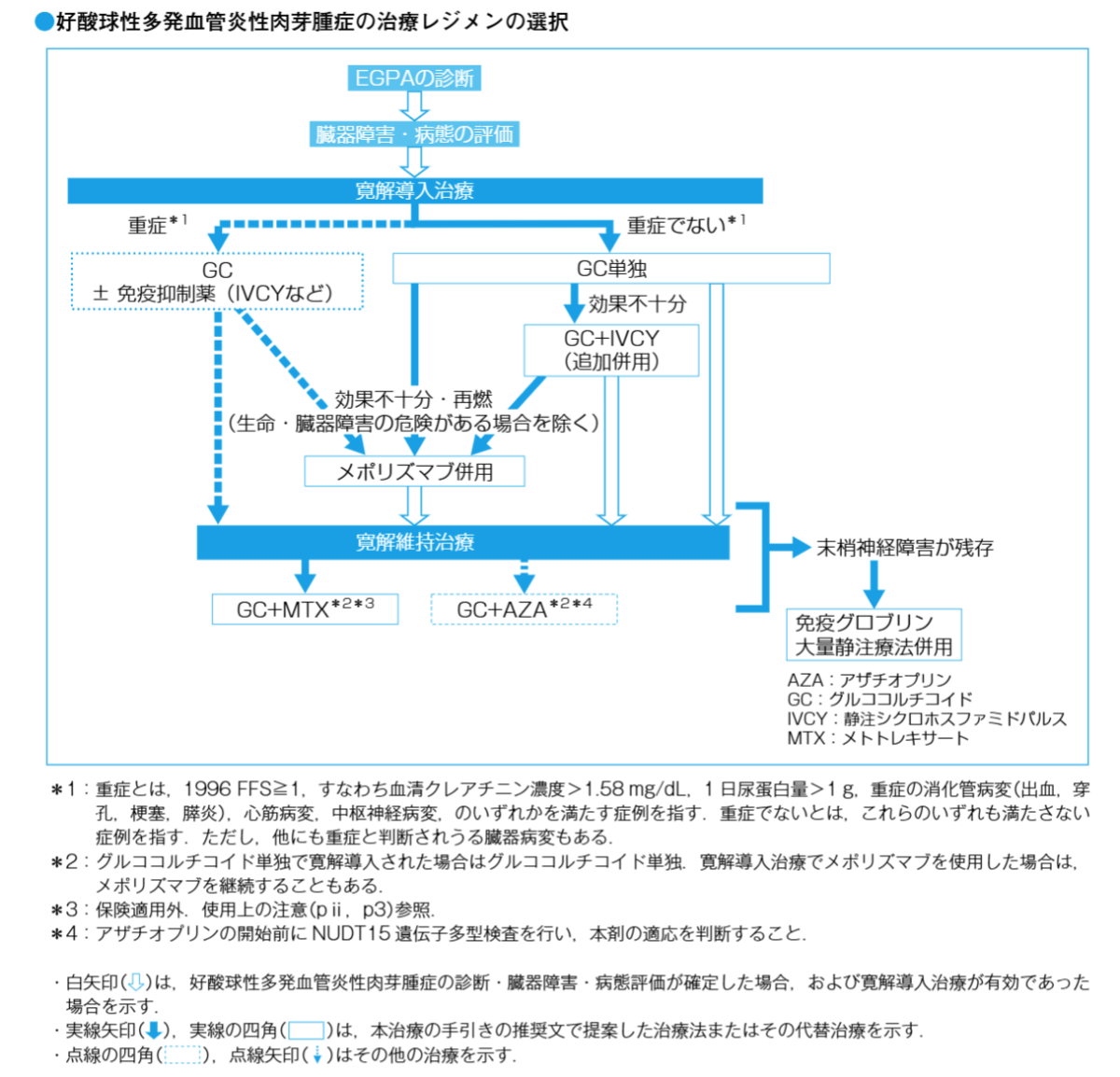
*抗リン脂質抗体症候群・好酸球性多発血管炎性肉芽腫症・結節性多発動脈炎・リウマトイド血管炎の治療の手引き 2020
EULAR 2022
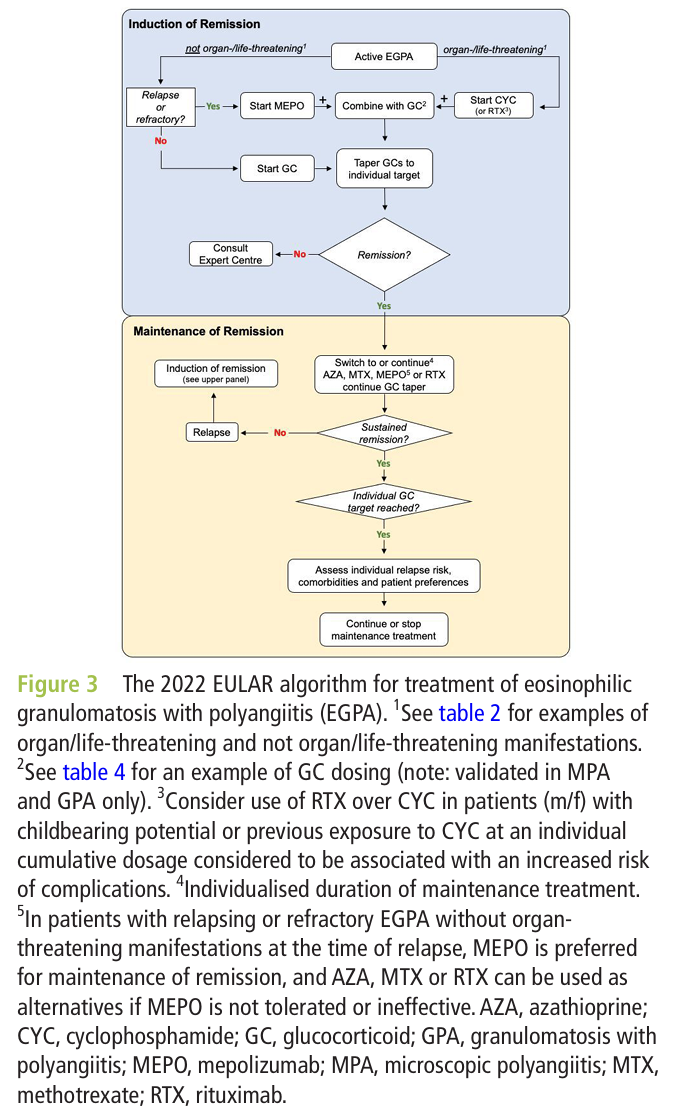
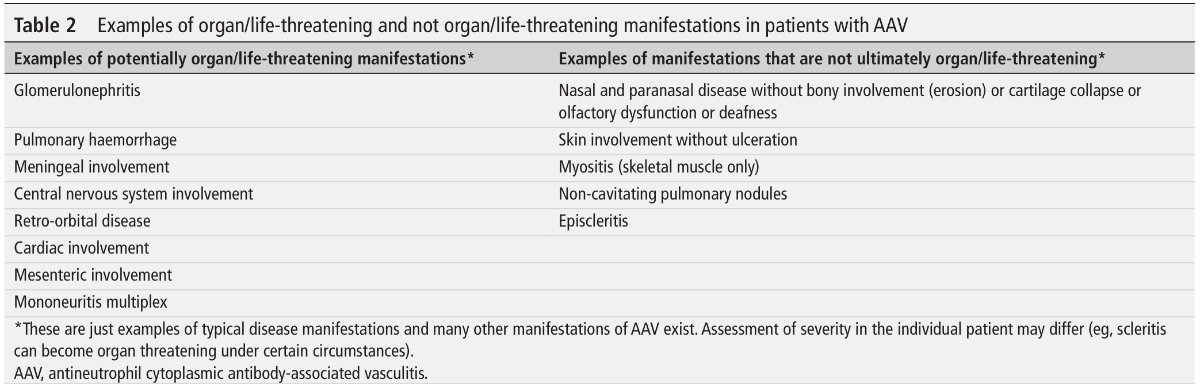
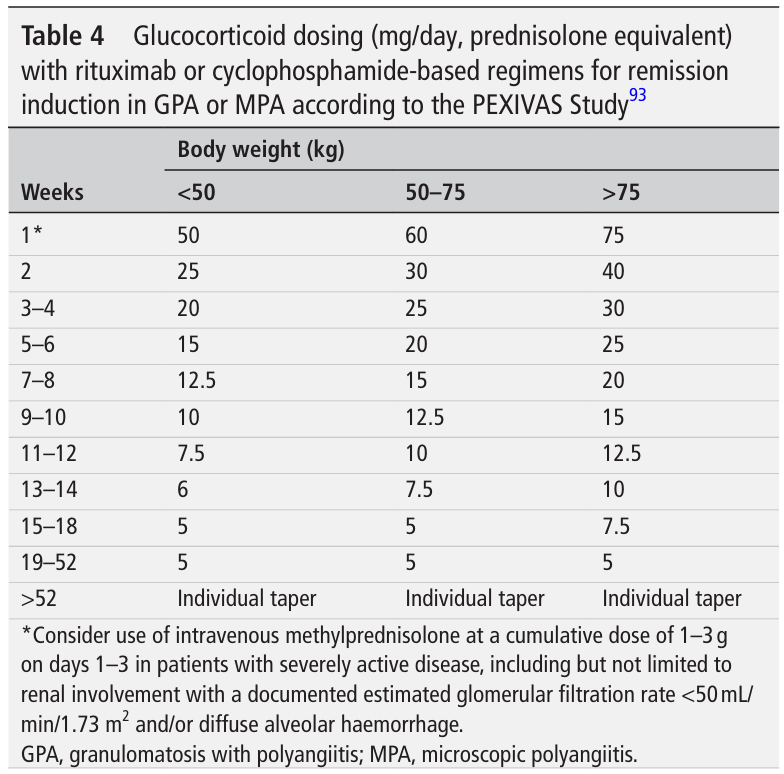
*Ann Rheum Dis. 2024;83(1):30-47.
引用・参考文献
Allergol Int. 2019;68(4):430-436.
Ann Rheum Dis. 2022;81(3):309-314.
Nat Rev Rheumatol. 2023;19(6):378-393.
Rheumatology. 2020;59(Suppl 3):iii84-iii94.
Allergol Int. 2019;68(4):430-436.
Autoimmun Rev. 2023;22(1):103219.
抗リン脂質抗体症候群・好酸球性多発血管炎性肉芽腫症・結節性多発動脈炎・リウマトイド血管炎の治療の手引き 2020
Ann Rheum Dis. 2024;83(1):30-47.